Kernidee
De mucuslaag in de darm is geen passieve beschermlaag, maar een dynamisch systeem dat continu wordt opgebouwd, afgebroken en gereguleerd door interacties tussen voeding, microbiota en metabolieten. Deze laag bepaalt in belangrijke mate hoe het immuunsysteem en de stofwisseling reageren op wat we eten.
Abstract
Voeding beïnvloedt de darm niet rechtstreeks, maar via microbiële processen. Fermenteerbare substraten worden door bacteriën omgezet in metabolieten zoals korte keten vetzuren. Deze metabolieten sturen de productie en stabiliteit van de mucuslaag, die op haar beurt bepaalt hoe dicht bacteriën bij het darmepitheel komen. Wanneer deze scheiding afneemt, neemt de blootstelling aan bacteriële componenten toe, wat gepaard kan gaan met verhoogde immuunactiviteit.
Deze verhoogde interactie leidt tot een toename van endotoxine-translocatie, wat resulteert in een verhoogde inflammatoire signaalactivatie. Deze publicatie beschrijft deze keten vanuit een mechanistisch perspectief, met aandacht voor zowel opbouw als verstoring.
Introductie
Discussies over voeding blijven vaak hangen in termen zoals gezond of ongezond, natuurlijk of bewerkt. Deze indeling beschrijft echter niet hoe het lichaam effectief reageert. Het lichaam verwerkt geen labels, maar signalen. Deze signalen worden in belangrijke mate gemedieerd door het microbioom en de structuren waarmee het in contact staat.
De mucuslaag in de darm vormt een van die structuren. Ze bepaalt niet alleen bescherming, maar ook communicatie. Om de rol van voeding te begrijpen, moet deze laag daarom bekeken worden als een actief systeem, niet als een statische barrière.
In dit artikel
- Hoe voeding de microbiële activiteit beïnvloedt
- Hoe metabolieten de mucuslaag sturen
- Hoe de mucuslaag interactie met het immuunsysteem bepaalt
- Hoe verstoringen in deze keten leiden tot systemische effecten
Context en probleemstelling
Binnen voedingscommunicatie wordt de darm vaak gereduceerd tot een plaats van vertering of tot een abstract begrip zoals darmgezondheid. Daarbij wordt zelden uitgelegd via welke processen voeding daadwerkelijk invloed uitoefent.
Ook wordt de mucuslaag meestal voorgesteld als een beschermende laag die schade voorkomt. Deze voorstelling is onvolledig. De mucuslaag is geen passieve structuur, maar een dynamisch evenwicht tussen productie, afbraak en microbiële interactie.
Het ontbreken van deze mechanistische uitleg leidt tot vereenvoudigde conclusies en absolute uitspraken die niet overeenkomen met de biologische realiteit.
Analyse
Voeding levert substraten die niet volledig door het lichaam zelf worden verwerkt. In de dikke darm worden deze substraten, voornamelijk fermenteerbare vezels, gebruikt door bacteriën.
Deze bacteriële fermentatie leidt tot de productie van korte keten vetzuren zoals butyraat, propionaat en acetaat. Deze moleculen functioneren als energiebron voor darmcellen en als signaalmoleculen die de activiteit van deze cellen beïnvloeden.
Butyraat speelt hierin een centrale rol. Het ondersteunt de energievoorziening van het darmepitheel en stimuleert de productie van mucines, de eiwitten waaruit de mucuslaag bestaat.
De mucuslaag wordt continu opgebouwd door epitheelcellen en tegelijkertijd afgebroken door specifieke bacteriën die deze structuren gebruiken als energiebron. Dit betekent dat de dikte en kwaliteit van de mucuslaag het resultaat zijn van een dynamisch evenwicht.
Wanneer dit evenwicht verschuift, verandert de afstand tussen bacteriën en het darmepitheel. In een stabiele situatie blijven bacteriën grotendeels gescheiden van de darmwand. Wanneer deze scheiding afneemt, neemt de interactie toe.
Bepaalde voedingscomponenten kunnen deze interactie beïnvloeden. In experimentele modellen is aangetoond dat sommige emulgatoren de relatie tussen microbiota en mucuslaag kunnen verstoren, waardoor bacteriën dichter bij het epitheel komen.
Deze verhoogde nabijheid leidt tot een grotere blootstelling van het immuunsysteem aan bacteriële componenten, zoals lipopolysacchariden. Dit resulteert niet in acute ontsteking, maar in een chronische, lage activatie van het immuunsysteem.
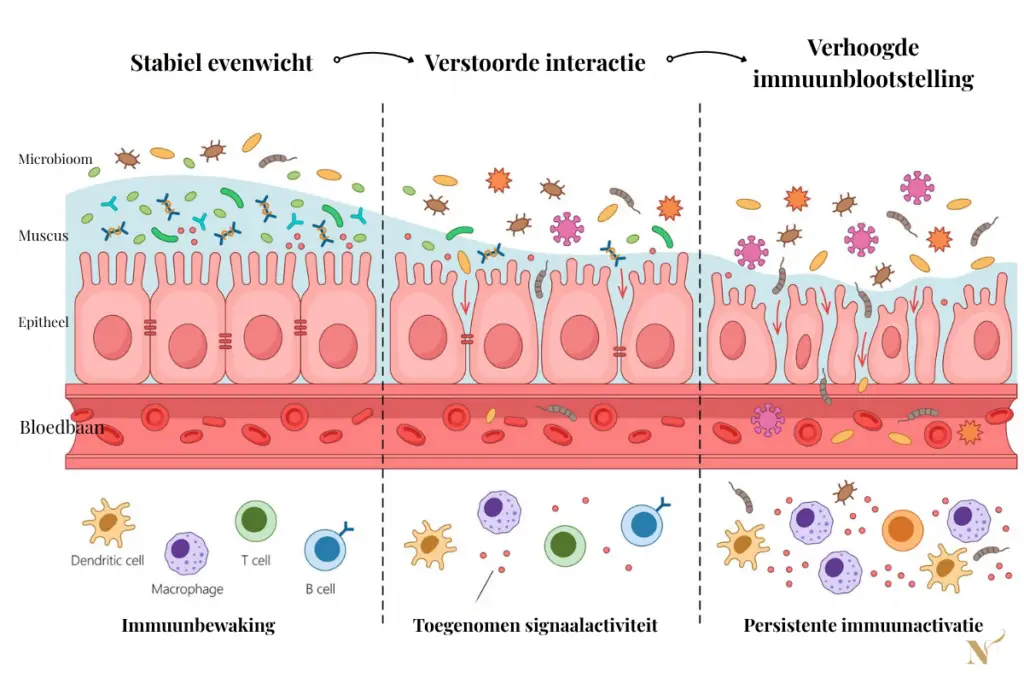
Lees dit schema van links naar rechts.
Links zie je een stabiel evenwicht waarbij de mucuslaag de afstand bewaart tussen microbiota en darmepitheel. De interactie met het immuunsysteem blijft beperkt.
In het midden verschuift dit evenwicht. Microbiële activiteit en afbraak van de mucuslaag nemen toe, waardoor bacteriën dichter bij het epitheel komen.
Rechts leidt deze verhoogde nabijheid tot een grotere blootstelling van het immuunsysteem aan bacteriële componenten, met een toename van immuunactivatie als gevolg.
Systeemdenken
De beschreven processen functioneren niet lineair, maar als een dynamisch systeem waarin meerdere lagen elkaar continu beïnvloeden.
Binnen het microbioomsysteem (MIC) bepalen bacteriële processen welke metabolieten worden geproduceerd. Deze metabolieten sturen de opbouw en afbraak van de mucuslaag. De toestand van deze mucuslaag bepaalt op haar beurt welke bacteriën zich kunnen handhaven en hoe dicht ze bij het darmepitheel komen.
Hier ontstaat een eerste terugkoppeling: de microbiële activiteit beïnvloedt de mucuslaag, terwijl de mucuslaag tegelijk de samenstelling en activiteit van de microbiota selecteert. Dit maakt de mucuslaag tot een regulerend mechanisme binnen het systeem, niet louter een beschermende structuur.
Wanneer de afstand tussen microbiota en epitheel afneemt, neemt de blootstelling van het immuunsysteem aan bacteriële componenten toe. Dit activeert het immuunsysteem (IMM), wat leidt tot een gewijzigde immuunrespons in de darmomgeving.
Deze immuunactivatie werkt vervolgens terug op het microbioom. Veranderingen in immuunactiviteit beïnvloeden welke bacteriën zich kunnen handhaven, waardoor de microbiële samenstelling opnieuw verschuift. Dit vormt een tweede terugkoppeling binnen het systeem.
Daarnaast heeft immuunactivatie invloed op metabole processen (MET), zoals insulinegevoeligheid en energieverdeling. Deze metabole veranderingen beïnvloeden de fysiologische toestand van het darmepitheel en kunnen zo indirect de productie en stabiliteit van de mucuslaag mee sturen.
Hierdoor ontstaat een gekoppeld systeem van terugkoppelingen:
microbiota → metabolieten → mucuslaag → immuunactivatie → microbiota
en
immuunactivatie → metabolisme → darmomgeving → mucuslaag
De mucuslaag functioneert binnen dit geheel als een interface waar meerdere systemen samenkomen. Ze reguleert niet alleen fysieke bescherming, maar ook de intensiteit en richting van signalen tussen microbiota, immuunsysteem en metabolisme.
Gezondheid binnen dit systeem is geen statisch evenwicht, maar het resultaat van continue aanpassing. Kleine verschuivingen in één onderdeel kunnen via deze terugkoppelingen versterkt of afgezwakt worden, afhankelijk van de context.
Institutionele implicaties
Binnen zorgcontexten zoals woonzorgcentra, ziekenhuizen en revalidatieomgevingen wordt voeding vaak beoordeeld op basis van samenstelling en voedingswaarde, zonder rekening te houden met deze procesmatige interacties.
Wanneer de rol van microbiota en mucuslaag niet wordt meegenomen, blijven interventies beperkt tot symptoombestrijding of algemene richtlijnen.
Een mechanistisch begrip maakt het mogelijk om voeding te evalueren op basis van haar effect op processen, eerder dan op basis van categorieën zoals gezond of ongezond.
Reflectie
De focus op voedingsmiddelen en labels maskeert de onderliggende processen die gezondheid bepalen. Door voeding te benaderen als signaalinput in een biologisch systeem, verschuift de aandacht van wat gegeten wordt naar wat het lichaam ermee doet.
De mucuslaag toont hoe deze benadering leidt tot een andere interpretatie van dezelfde voedingskeuzes.
Beperkingen van deze analyse
Een groot deel van de beschikbare data over de invloed van emulgatoren en microbiota-interacties is gebaseerd op diermodellen. Humane studies zijn beperkter en tonen variabiliteit afhankelijk van individuele microbiota-samenstelling.
Daarnaast zijn de effecten van voeding sterk afhankelijk van context, waaronder dieetpatroon, leeftijd en gezondheidstoestand.
Observatiestatus
Deze analyse is gebaseerd op een combinatie van literatuurstudie en conceptuele modellering binnen het kader van systeemdenken. Verdere validatie in specifieke doelgroepen, zoals ouderen en revalidatiepatiënten, is noodzakelijk.
Referenties
Chassaing, B., et al. (2015). Dietary emulsifiers impact the mouse gut microbiota. Nature
Koh, A., et al. (2016). From dietary fiber to host physiology. Cell
Makki, K., et al. (2018). The impact of dietary fiber on gut microbiota. Cell Host & Microbe
Johansson, M. E. V., et al. (2013). The inner of the two mucus layers in colon. PNAS
Cani, P. D., et al. (2007). Metabolic endotoxemia. Diabetes
Belkaid, Y., & Hand, T. (2014). Role of the microbiota in immunity. Cell
Hall, K. D., et al. (2019). Ultra-processed diets. Cell Metabolism
Gerelateerde publicaties
Voeding als sturing van vettransport en vaatreactie
Nieuwe studie: het microbioom
Metabole signalen en gewichtsregulatie
