Kernidee
Slaap is geen rustmoment, maar een actieve fase waarin het lichaam zijn interne timing, de biologische klok (circadiaanse 24-uursregeling), gebruikt om herstelprocessen te sturen en signalen opnieuw af te stemmen.
Abstract
Tijdens de slaap verschuift de hormonale aansturing van het lichaam. Melatonine neemt toe en zet het lichaam in een nachtfase, terwijl cortisol juist daalt en pas tegen de ochtend opnieuw stijgt. Tegelijk worden andere signalen, zoals insuline, minder actief, waardoor energie minder naar opslag gaat en meer beschikbaar blijft voor herstelprocessen. In die context krijgt somatotropine (groeihormoon) meer ruimte, somatotropine dat tijdens de slaap vrijkomt en herstel van weefsels ondersteunt.
Introductie
Slaap wordt vaak beschouwd als een periode van rust. Biologisch gezien is dit onjuist.
Tijdens de slaap verschuift de hormonale balans fundamenteel. Deze verschuiving bepaalt of het lichaam zich op herstel, of onder invloed blijft van aanhoudende belasting.
Wie slaap reduceert tot “voldoende uren”, mist het mechanisme dat bepaalt wat er tijdens die uren gebeurt.
Context en probleemstelling
Slaaptekort wordt meestal gekoppeld aan vermoeidheid. Dat is een symptoom, geen verklaring.
De kern ligt in de hormonale regulatie. Wanneer deze verstoord raakt:
- worden herstelprocessen onvolledig uitgevoerd
- verschuift het lichaam naar een katabole toestand (afbraak)
- stapelen beschadigingen zich op
Dit effect is vaak niet onmiddellijk zichtbaar, maar wel meetbaar op langere termijn.
Analyse
1. Hormonale verschuiving als startpunt
Tijdens de slaap verandert de verhouding tussen meerdere hormonen, waarvan drie een centrale rol spelen:
- Melatonine stijgt → signaal voor herstel en circadiaanse synchronisatie
- Cortisol daalt → remming van afbraakprocessen
- Somatotropine stijgt → activatie van weefselherstel
Deze combinatie creëert een fysiologische toestand waarin herstel mogelijk wordt.
Mechanistische koppeling:
- Somatotropine (GH) stimuleert de aanmaak van IGF-1 (insuline-like growth factor 1) in de lever
- IGF-1 bevordert:
- eiwitsynthese
- celgroei
- herstel van spier- en bindweefsel
Wanneer cortisol verhoogd blijft (stress, slechte slaap):
- blijft gluconeogenese (aanmaak van glucose) actief
- wordt eiwitafbraak gestimuleerd
- wordt herstel geremd
Het lichaam blijft dan in een toestand van paraatheid in plaats van herstel.
2. Celherstel en autofagie (nuancering)
Tijdens de slaap worden omstandigheden gecreëerd die celherstel ondersteunen.
Een belangrijk proces hierbij is autofagie
(= het afbreken en recycleren van beschadigde celonderdelen)
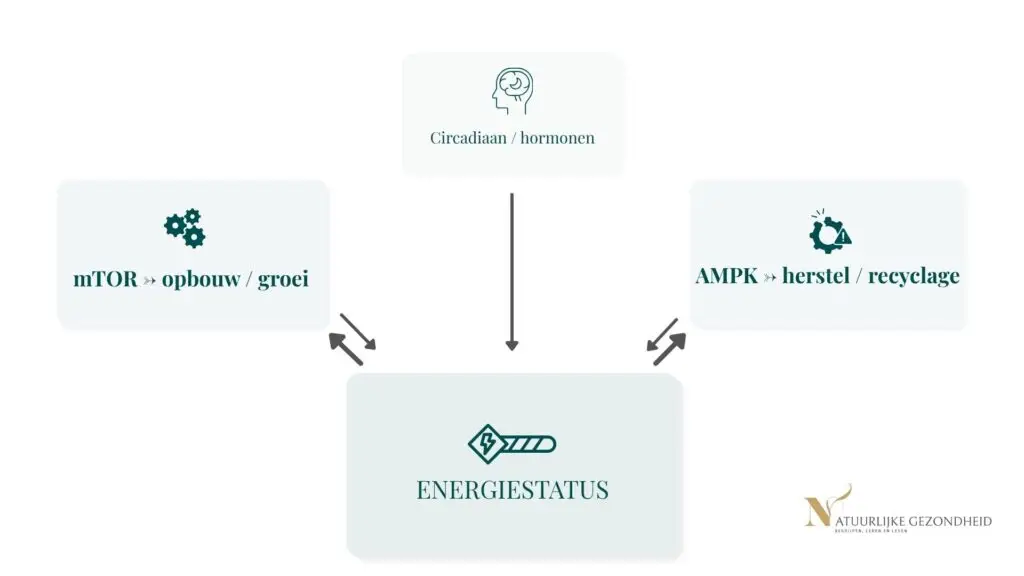
Autofagie wordt vooral gestuurd door de energietoestand van de cel en de beschikbaarheid van voedingsstoffen.
- energiestatus van de cel (AMPK/mTOR-signaalroutes)
- nutriëntbeschikbaarheid
- cellulaire stress
Dit gebeurt via interne signaalroutes die bepalen of de cel opbouwt of opruimt. Slaap speelt hierin een ondersteunende rol, maar is niet de primaire trigger.
Wat doet slaap dan wél?
- verlaagt cortisol → minder remming van herstel
- stabiliseert energiebalans
- ondersteunt mitochondriale functie
Bij verstoorde slaap:
- blijft stresssignalisatie actief
- wordt celreiniging minder efficiënt
- stapelen beschadigde eiwitten zich op
3. Immuunregulatie
Tijdens de slaap wordt het immuunsysteem actief gestuurd via hormonale en neuronale signalen.
Belangrijke mechanismen:
- regulatie van cytokines
(= signaalstoffen tussen immuuncellen) - activatie en differentiatie van immuuncellen
- controle van ontstekingsreacties
Bij voldoende slaap:
- ontstaat een gecontroleerde immuunrespons
- wordt herstel van weefselschade ondersteund
Bij chronisch slaaptekort:
- stijgt ontstekingsactiviteit (laaggradige inflammatie)
- daalt de efficiëntie van immuunrespons
Dit is objectief meetbaar via ontstekingsmarkers zoals CRP.
4. Energiebalans en metabolische regulatie
Slaap beïnvloedt direct hoe het lichaam energie verwerkt.
Hormonale regulatie stuurt:
- glucosegebruik → gestuurd door insuline en cortisol, die bepalen hoeveel glucose wordt opgenomen of vrijgemaakt
- insulinegevoeligheid → beïnvloed door cortisol en slaapkwaliteit, wat bepaalt hoe efficiënt cellen reageren op insuline
- vetopslag en vetverbranding → gestuurd door insuline (opslag) en groeihormoon (vrijmaken van energie uit vet)
- eetlustsignalen → gereguleerd door ghreline (hongersignaal) en leptine (verzadigingssignaal)
Mechanisme:
- verhoogd cortisol → verhoogde gluconeogenese, dit is het proces waarbij het lichaam zelf nieuwe glucose (suiker) aanmaakt uit niet-koolhydraatbronnen, zoals aminozuren, glycerol en melkzuur.
- verminderde slaap → lagere insulinegevoeligheid
Gevolg:
- verhoogde bloedsuiker
- verschuiving naar vetopslag
- verhoogde eetlust (via ghreline/leptine verstoring)
Dit verklaart waarom slaaptekort samenhangt met metabole ontregeling, zelfs zonder verandering in voeding.
Voedingskoppeling (beperkt maar essentieel)
Hoewel slaap primair een regulatieproces is, beïnvloedt voeding dit mechanisme direct:
- Tryptofaanrijke voeding (bv. eieren, vis) ondersteunt melatoninesynthese
- Alcohol verstoort slaaparchitectuur en REM-slaap
- Late glucosepieken kunnen cortisolregulatie verstoren
Voeding beïnvloedt dus de hormonale omgeving waarin slaap zijn werk moet doen.
Systeemdenken
Slaap stuurt niet één functie, maar meerdere processen tegelijk. Wanneer de hormonale aansturing tijdens de nacht verschuift, beïnvloedt dit gelijktijdig hoe het lichaam herstelt, hoe het immuunsysteem reageert en hoe energie wordt verdeeld.
Somatotropine (GH) ondersteunt het herstel van weefsels, terwijl veranderingen in cortisol en insuline bepalen hoe energie wordt vrijgemaakt of opgeslagen. Tegelijk worden immuunsignalen afgestemd, waardoor het lichaam gerichter kan reageren op beschadiging of belasting.
Deze gelijktijdige aansturing maakt duidelijk dat slaap geen afzonderlijke factor is, maar een centrale regelaar die meerdere functies in het lichaam met elkaar verbindt.
Institutionele implicaties
In veel omgevingen wordt slaap structureel ondermijnd:
- ploegensystemen
- nachtwerk
- chronische stress
- onregelmatige ritmes
Gevolg:
- verstoorde hormonale regulatie
- trager herstel
- verminderde prestaties
Een systeemgerichte aanpak vraagt daarom:
structurele aanpassingen, niet enkel gedragsadvies
Reflectie
Het idee dat slaap automatisch leidt tot herstel is misleidend. Herstel ontstaat alleen wanneer hormonale signalen en energieregulatie tijdens de slaap correct op elkaar afgestemd zijn.
Voeding speelt hierin een rol, maar niet als directe oplossing. Nutriënten zoals tryptofaan, magnesium en polyfenolen ondersteunen processen, maar vervangen geen correcte regulatie.
Beperkingen
De interactie tussen processen is complex en afhankelijk van context
Individuele variatie (leeftijd, stressniveau, leefstijl) beïnvloedt de uitkomst
Veel studies zijn uitgevoerd in gecontroleerde omstandigheden en vertalen niet altijd één-op-één naar dagelijkse situaties
Observatiestatus
De beschreven hormonale en metabole reacties tijdens de slaap zijn gebaseerd op goed onderbouwde fysiologische kennis. De samenhang tussen deze signalen, zoals hier beschreven, is een analytische interpretatie die helpt om hun gecombineerde effect op herstel en energiebalans beter te begrijpen.
Referenties (APA)
Van Cauter, E., & Plat, L. (1996). Physiology of growth hormone secretion during sleep. Journal of Pediatrics, 128(5), S32–S37.
Spiegel, K., Leproult, R., & Van Cauter, E. (1999). Impact of sleep debt on metabolic and endocrine function. The Lancet, 354(9188), 1435–1439.
Irwin, M. R. (2015). Why sleep is important for health: A psychoneuroimmunology perspective. Annual Review of Psychology, 66, 143–172.
Mattson, M. P., Longo, V. D., & Harvie, M. (2017). Impact of intermittent fasting on health and disease processes. Ageing Research Reviews, 39, 46–58.
Walker, M. (2017). Why We Sleep. Scribner.
Gerelateerde publicaties
Kernboodschap
Slaap stuurt via hormonale regulatie gelijktijdig celherstel, immuunfunctie en energiebalans aan.
